氯化铝为什么是共价化合物因为氯化铝在水溶液里或熔融状态下不能电离出离子 , 所以是共价化合物
氧化铝在熔融状态下可以电离出铝离子和氧负离子,所以是离子化合物
alcl3为什么是共价化合物原因如下:
因为alcl3中不存在孤立的铝离子和氯离子 , 而是存在Al与Cl的共价键与配位键 , 所以氯化铝是共价化合物 。而共价化合物是通过共用电子构成的共价键结合而成的化合物 。由于AlCl3中存在Cl上的孤对电子向旁边的Al进行配位,故AlCl3以多聚体的形式存在(AI2CI6 ),形成共价化合物更稳定 。
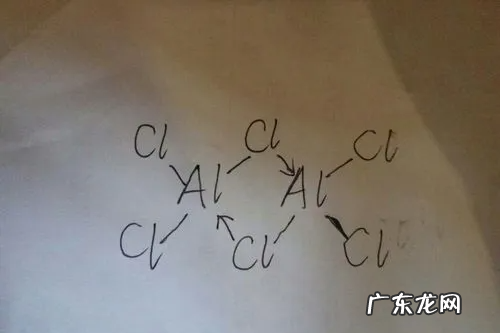
文章插图
ALCL3的物化性质:
氯化铝,白色结晶性粉末,有强盐酸气味,工业品呈淡黄色 。易溶于水、醇、氯仿、四氯化碳,微溶于苯 。熔化的氯化铝不易导电 , 和大多数含卤素离子的盐类(如氯化钠)不同 。氯化铝的水溶液完全解离,是良好的导电体 。
氯化铝在178℃升华,它的蒸气是缔合的双分子 。在空气中能吸收水分,一部分水解而放出氯化氢 。
以上内容参考:
为什么氯化铝是共价化合物氯化铝是共价化合物的原因:因为铝电荷高,半径小,所以极化力较强,使得它与氯的化学键为共价键 。
氯化铝是共价化合物 , 因为铝电荷高 , 半径?。?所以极化力较强,使得它与氯的化学键为共价键 。另外Al2Cl6分子中严格来说没有配位键,是三电子两中心的氯桥键 。
从价键理论的观点(价键理论要求两个原子之间通过各自提供一个满足要求的原子轨道的重叠来形成共价键)看,氯桥键属于共价键范畴 。所以Al2Cl6是共价化合物 。至于电负性 , 那只是用来根据化学式推断某简单二元化合物是否是共价化合物的一个工具而已,不足以作为依据 。

文章插图
两个原子结合,是以共价键形式还是以离子键形式,主要取决于两个原子的电负性差值 。电负性差值很大的金属和非金属结合,以离子键为主 。电负性差值小的两个非金属结合 , 以共价键为主 。
共价化合物的特点:
1、由相同元素原子组成的分子其共用电子对无偏移 。单质的共用各原子不带电性,称为单质的分子,如氧气的分子 。

文章插图
2、由不同元素的原子组成的分子由其共用电子对有偏移(偏向非金属较强的元素原子一方),使双方带相反的电性 , 但没有电子得失,故化合物中不存在离子 。整个分子仍是电中性 。
3、有些共价化合物 , 其共用电子对偏移程度大 , 在水溶液中能形成阴、阳离子 。例如:HCI→H++Cl-,非金属元素原子间的反应,一般形成共价化合物 。
AlCl3为什么是共价化合物这个是看极化,变形性质的
Al3+由于带的电荷多,并且原本半径就?。?使得它的正电荷密度很高
而Cl-半径大,核外电子多,带的负电荷密度也很大
这样当两者遇到一起的时候,Al3+显示出了强大的极化性,Cl-显示出强大的变形性,即Cl-的电子云被Al3+扭曲变性偏向了Al3+
这样就使得Al3+的电性被中和了一些,而不是电子的得失这么简单,而是电子云的偏移,具有共价键的性质,所以说它是共价化合物
【氯化铝为什么是共价化合物,alcl3为什么是共价化合物】
- 澳大利亚被称为什么 澳大利亚被称为什么大陆
- 主干家庭是指 主干家庭是指父母和一对已婚子女组成的家庭
- 爆炸品禁止使用的灭火剂是什么为什么 爆炸品禁止使用的灭火剂是什么
- 韩国财阀是什么意思,韩国财阀千金什么意思
- 建安的时代特点是什么,建安时代的诗歌有哪些特点
- 水银的凝固点是多少,水银温度计打碎怎么处理干净
- gbt20823是什么标准,GBT20823是什么酒
- 大米营养功效与作用是什么 大米营养
- 微波炉煮饭的方法,微波炉煮饭快捷方便的烹饪方式是什么
- 离婚协议做公证需要哪些手续,办理离婚协议书公证是在离婚前
特别声明:本站内容均来自网友提供或互联网,仅供参考,请勿用于商业和其他非法用途。如果侵犯了您的权益请与我们联系,我们将在24小时内删除。
