此前 , 仅美国批准的再生元公司鸡尾酒综合抗体在临床试验中降低轻症病人病毒载量2.5倍(降低0.41 log10拷贝/毫升) 。
目前 , 针对无症状、轻型以及普通型新冠肺炎的III期临床试验亦在进行中 。 刘龙斌表示 , “治疗无症状至普通型新冠的III期临床研究”于2021年8月紧急启动 , 中国科学院院士、国家感染性疾病临床医学研究中心主任、国务院联防联控机制科研攻关专家组专家王福生院士牵头 , 主要观察乐复能治疗后病毒转阴数据(以观察感染德尔塔变异株的患者为主) , 为探讨乐复能用于我国预防和治疗新冠的“防治结合”策略 , 提供科学数据和依据 。 预计入组病人200例左右 , 该研究正在进行中 , 主要收集口岸医院的患者 , 已观察20多例患者 。
另外关于“治疗非住院的轻型新冠的III期临床研究” , 由日本研究者发起 , 刚获得日本厚生省旗下药监部门-PMDA紧急批准 , 预计入组200例左右 , 11月初启动 。
3期临床试验的药物们
新冠肺炎的持续流行 , 使得人们不得不重新审视原本希望通过疫苗接种达到群体免疫 , 进而消除病毒传播的乐观想法 。
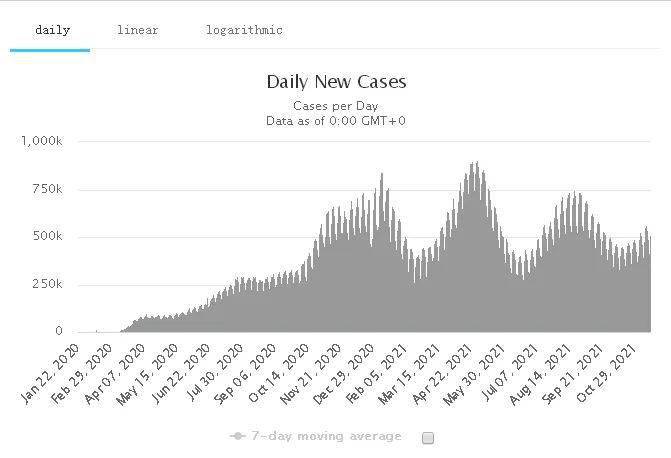
据Worldometers数据 , 截至11月18日1:06 , ,全球新冠确诊病例达到255,672,242例 , 死亡5,137,834例 。 单日新增确诊577,526例 。
文章图片
全球单日新增确诊病例 。 来源:Worldometers
陈凯先在上述峰会上表示 , 在许多国家和地区疫苗接种已有一定覆盖率的情况下 , 仍引起新一轮疫情 , 这突显了抗新冠肺炎特效药物研发的重要性和紧迫感 , 特效药物是战胜疫情、消除恐慌、保护人类的终极武器 。
【全球新冠药物赛道渐明朗:上百个三期临床,谁能胜出?】为了尽快找到有效治疗方法 , 世界卫生组织牵头发起了全球层面的团结试验 , 旨在比较药物的安全性和有效性 。
寻找新冠特效药物的主要路径有两条:一类是生物大分子药物 , 以抗体类药物为主 , 该类药物全球研发进展较快 , 但对变异病毒株效果较差 , 且成本高、注射使用不方便 。 另一类则是小分子药物 , 可抑制病毒浸入、复制环节 , 该类药物对各种变异株均有广谱作用 , 具有可居家口服治疗、易于迅速启动大规模生产应急供应、成本低、可及性好、适合大范围人群使用等优点 , 成为各国加快研发抗新冠肺炎特效药的集中发力点 。
在全球在研抗新冠肺炎候选小分子药物中 , 进展较快的有开拓药业的普克鲁胺、中科院上海药物所的DC402234和VV936、默沙东的核苷类抗病毒药物EIDD-2801、辉瑞公司的口服新冠病毒主蛋白酶抑制剂PF-07321332等 。
其中7个处于III期临床试验的新冠药物比较受关注 , 分别是吉利德公司的瑞德西韦(已获批 , 年销售50多亿美元);默沙东公司的莫努匹韦(通过EUA(应急使用授权)申请方式 , 首获英国上市批准);辉瑞公司的口服抗病毒蛋白酶抑制剂PF-07321332(3期临床中期数据揭盲);盐野义公司的口服抗病毒蛋白酶抑制剂S-217622(1期临床结束 , 2/3期临床9月下旬启动);罗氏公司的RNA聚合酶抑制剂AT-527(2期临床失败);杰华生物的广谱抗病毒药物乐复能(4个3期临床中 , 已经获得有效数据);开拓药业的雄激素受体拮抗剂普克鲁胺(3期临床) 。
这些关注度高的新冠药物 , 研究数据如何?
瑞德西韦主要用于重症住院患者 , 其获益指标为“缩短住院时间4天” , 病毒清除时间未披露;
再生元中和抗体(鸡尾酒疗法)主要用于轻、中度非住院患者 , 主要或死亡减少70% , 可降低病毒载量0.41Log10拷贝/毫升 , 缩短症状缓解时间5-7天;
特别声明:本站内容均来自网友提供或互联网,仅供参考,请勿用于商业和其他非法用途。如果侵犯了您的权益请与我们联系,我们将在24小时内删除。
